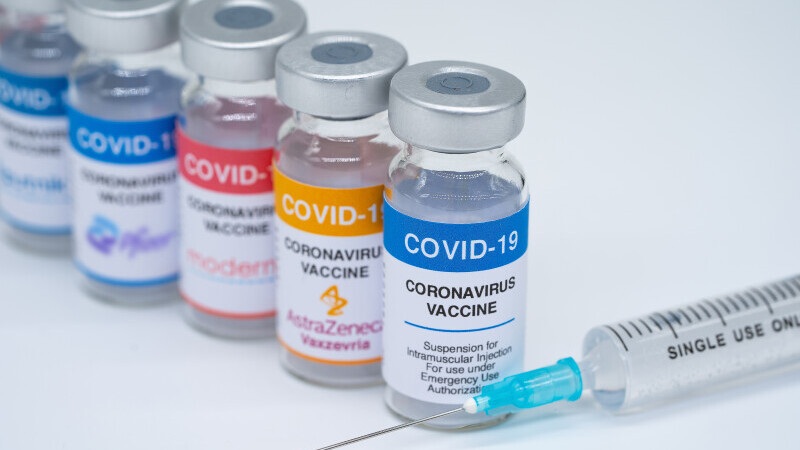
Pfizer testează folosirea unui vaccin pneumocic împreună cu o a treia doză de vaccin pentru Covid-19

Pfizer a anunţat luni că a început un studiu clinic care constă în administrarea unui vaccin pneumocic candidat împreună cu o a treia doză de vaccin Pfizer-BioNTech pentru Covid-19, la persoane cu vârste de peste 65 de ani, transmite Reuters.
Obiectivul studiului este de a înţelege dacă această combinaţie de vaccinuri este sigură şi reacţia sistemului imunitar după adăugarea unui vaccin pneumococic la vaccinul pentru Covid-19, potrivit Pfizer, citat de News.ro.
Vaccinul pneumococic candidat, 20vPnC, este dezvoltat pentru protejarea adulţilor împotriva a 20 de serotipuri responsabile de majoritatea bolilor pneumoccocice invazive şi pneumonie.
Noul studiu va include 600 de adulţi care vor fi recrutaţi din studiul pentru vaccinul pentru Covid-19, în stadiu târziu, al celor două companii, după ce aceştia au primit a doua doză de vaccin cu cel puţin şase luni înainte de a intra în studiul de co-administrare.
S-a recomandat anterior că vaccinurile pentru Covid-19 sunt sigure pentru a fi administrare singure. Dar, pe baza experienţei cu vaccinuri non-Covid, Centrul SUA pentru Controlul şi Prevenirea Bolilor a declarat că vaccinurile COVID-19 şi alte vaccinuri pot fi administrate simultan sau în aceeaşi zi.
În decembrie, Administraţia americană pentru alimente şi medicamente (FDA) a acceptat să evalueze cu prioritate o cerere a Pfizer de licenţă pentru administrarea vaccinului 20vPnC la adulţi cu vârste de peste 18 ani şi a stabilit o dată pentru decizie în luna iunie.
Două luni mai târziu, Agenţia Europeană a Medicamentului (EMA) a acceptat cererea companiei de autorizare a introducerii pe piaţă a 20vPnC.